On utilise plus communément le terme de protéines pour nommer ces molécules, mais nous allons voir que les protéines ne sont qu'une catégorie de protides. Ce sont des molécules en général solubles dans l'eau et très sensibles à l'acidité de leur milieu. Les protides sont caractérisés par leur présence dans toutes les cellules, leur complexité structurale, leur abondance dans les êtres vivants et leur diversité fonctionnelle. Un protide est un polymère d'acides aminés.
Les acides aminés, de formule générale R-CH(NH2)(COOH), sont donc les protides de base. Dès que deux acides aminés sont liés, on parle de peptides (dipeptide, tripeptide...). A partir de quelques acides aminés, on parle de polypeptides et quand le nombre dépasse 20, on parle de protéines. Ainsi, il n'y a pas vraiment de classification des protides. On distingue les protéines par leur fonction :
- fonction de catalyse (exemple : toutes les enzymes)
- fonction de stockage (ex : caséine du lait...)
- fonction de transport (ex : hémoglobine du sang...)
- fonction de régulation (ex : toutes les hormones : insuline, adrénaline...)
- fonction de structure (ex : collagènes...)
- fonction de protection (ex : anticorps, fibrinogènes...)
- fonction de défense (ex : toutes les toxines : venin de serpent...)
3) La liaison peptidique
:
On appelle
ainsi la liaison chimique qui s'établit entre deux acides aminés. Une telle
liaison provoque le départ d'une molécule d'eau
(H2O) :
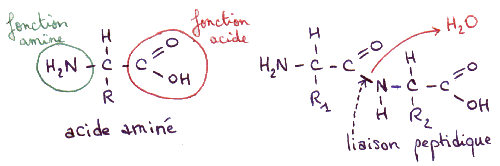
Une protéine peut ainsi être constituée de plusieurs centaines d'acides aminés mis bout à bout.
4) Les acides aminés :
Il existe
en fait 20 acides aminés différents chez les êtres vivants. En voici la liste
avec leur formule chimique et leur symbole :
| Nom | Abréviation et symbole | Formule |
| Glycine | Gly (G) | H-CH-COOH | NH2 |
| Alanine | Ala (A) | H3C-CH-COOH
| |
| Valine | Val (V) | (CH3)2-CH-COOH
| |
| Leucine | Leu (L) | (CH3)2-CH-CH2-CH-COOH
| |
| Isoleucine | Ile (I) | (CH2CH3)(CH3)CH-COOH
| |
| Sérine | Ser (S) | HOH2C-CH-COOH
| |
| Thréonine | Thr (T) | H3C-CH-CH-COOH
|
| |
| Cystéine | Cys (C) | HS-CH2-CH-COOH
| |
| Méthionine | Met (M) | CH3-S-(CH2)2-CH-COOH
| |
| Acide aspartique | Asp (D) | HOOC-CH2-CH-COOH
| |
| Asparagine | Asn (N) | O = C-CH2-CH-COOH
|
| |
| Acide glutamique | Glu (E) | HOOC-(CH2)2-CH-COOH
| |
| Glutamine | Gln (Q) | O = C-(CH2)2-CH-COOH
|
| |
| Lysine | Lys (K) | H2N-(CH2)4-CH-COOH
| |
| Arginine | Arg (R) | NH = C-NH-(CH2)3-CH-COOH
|
| |
| Phénylalanine | Phe (F) | 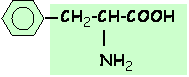 |
| Tyrosine | Tyr (Y) |  |
| Tryptophane | Trp (Y) |  |
| Histidine | His (H) | HC = C-CH2-CH-COOH
| |
|
\ // |
| Proline | Pro (P) | H2C - CH-COOH
| |
\ / |
Grâce à cette notation, on peut noter une protéine par sa séquence en acides aminés. Prenons l'exemple de l'ocytocine bovine, une hormone qui a un rôle sur les contractions de l'utérus : sa séquence est Cys-Tyr-Ile-Gln-Asn-Cys-Pro-Leu-Gly. C'est ce qu'on appelle la structure primaire des protéines. La structure secondaire est l'agencement dans l'espace des acides aminés les uns par rapport aux autres (formation de coudes ou de liaisons particulières). La structure tertiaire est l'agencement dans l'espace de la chaîne d'acides aminés (segments, domaines hydrophiles et hydrophobes...). Enfin, la structure quaternaire d'une protéine correspond à la disposition dans l'espace de ses sous-unités (plusieurs chaînes forment la protéine et d'autres molécules peuvent se greffer dessus).